Урок 30. Хлороводород и хлорная кислота
Химия. Онлайн учебник → Хлороводород и хлорная кислота
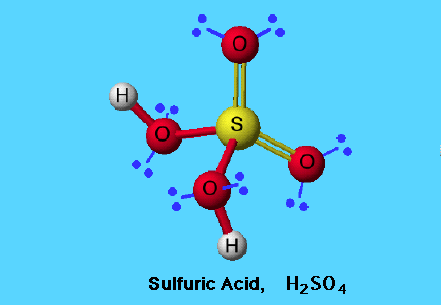
Получение хлороводорода и хлорной кислоты
В промышленности (горение водорода в атмосфере хлора):
H2 + Cl2 (t) = 2HCl
В лаборатории:
2NaCl(тв.) + H2SO4(конц.) (t) = 2HCl + Na2SO4
Хлороводород растворяют в воде и получают хлорную кислоту. Качественная реакция на хлорид ион Cl-. AgCl - бело-серый осадок:
HCl + AgNO3 = AgCl + HNO3
Ag+ + Cl- = AgCl
Применение хлороводорода, хлорной кислоты и хлоридов
| Производство органических веществ содержащих хлор | ||
| Переработка руд |
HCl |
Производство хлоридов |
| Очистка поверхности металлов от коррозии |
Получение Cl2 в лаборатории |
Осуществление гидролиза целлюлозы |
Производство соды, NaOH, Cl2, Na
| В сельском хозяйстве |
NaCl |
В пищевой промышленности |
| в быте (кулинария, консервация) | В смеси с песком зимой на дорогах |
В химической промышленности (осушитель газов, органических растворителей, производство кальция)
| В пищевой промышленности | CaCl2 | В медицине |
Для производства соляной кислоты, хлорной извести
| В качестве окислителя, во время производства органических и неорганических веществ | Cl2 |
Для отбеливания ткани, бумажной массы |
Для обеззараживания питьевой воды (хлорирования).
| Производство KOH | KCl | Минеральные удобрения |
Галогены (часть 1) (часть 2)
Автор: Гончаренко Л. И. (ula-books.com.ua)
< Урок 29 | Химия. Онлайн учебник | Урок 31 >
Смотрите также:
Количество вещества и молярная масса
Органические соединения. Ген. связь
Урок 76. Полимеры и пластмассы