Урок 44. Влияние атомов в молекулах органических соединений
Химия. Онлайн учебник → Влияние атомов в молекулах органических соединений
Взаимное влияние атомов или групп атомов в молекулах органических соединений
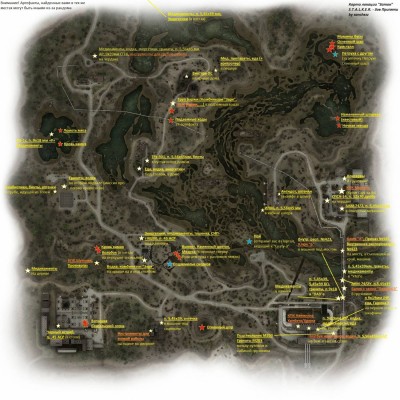
1. Присоединение галогеноводородов к пропену по правилу Марковникова (реакция соединения).
Во время присоединения веществ типа HX (где X - галогены, --OH) у несимметричных алкенов атом Водорода присоединяется к, связанному с большим числом атомов Водорода, атому Углерода с кратной связью. X - к атому содержащему наименьшее количество Водорода.
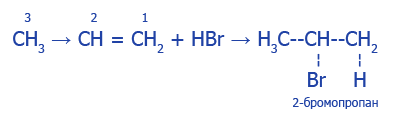
2. Присоединение воды к пропену по правилу Марковникова:
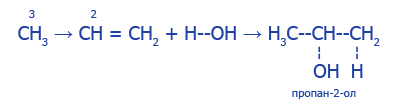
3. Спирты - нейтральные вещества, а реакции со щелочными металлами являются примером проявления спиртами кислотных свойств:
2C2H5OH + 2Na → 2C2H5ONa + H2
C2H5OH - этанол
C2H5ONa - этанолят натрия (этилат натрия)
4. Кислотные свойства у фенолов выражены больше, чем у спиртов. Это доводят реакции фенолов с водными растворами щелочей с созданием солей-фенолятов (одноатомные спирты создают алкоголяты только во время взаимодействия со щелочными металлами):
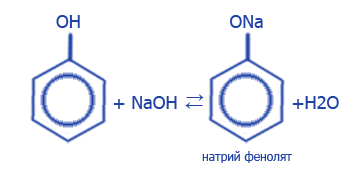
5. Гидроксильная группа у фенолов сильно активирует бензольное кольцо и помогает реакциям замещения атомов Водорода в орто- и пара-положениях.
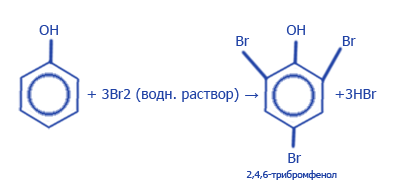
6. Все углеродные кислоты - слабые. С увеличением молекулярной массы сила кислот уменьшается. Если заменить атомы Водорода в углеводородном радикале на атомы более электроотрицательного элемента - галогена, сила кислоты, т.е. способность ее молекулы к отцеплению ионов H+, многократно увеличивается.
Все это - результат увеличения полярности связи O--H в результате перераспределения электронной густоты в молекуле под воздействием атома галогена. Перераспределение электронной густоты в молекулах кислот:
| Углеродная | Угольная кислота хлора |
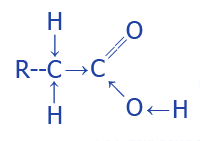 |
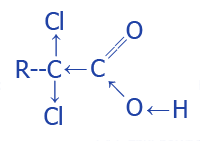 |
7. Реакция анилина с бромом. Благодаря неразделенной электронной паре атома Азота аминогруппа увеличивает электронную густоту в бензольном кольце и активирует его в орто- и пара-положениях. Анилин легко вступает в реакцию с бромной водой:

Основы органической химии (часть 1) (часть 2) (часть 3) (часть 4) (часть 5)
Автор: Гончаренко Л. И. (ula-books.com.ua)
< Урок 43 | Химия. Онлайн учебник | Урок 45 >
Смотрите также:
Способы получения карбоновых кислот
Урок 66. Эфиры. Жиры (часть 1)
Урок 62. Углеводы. Изомерия