Урок 35. Химические свойства NO2
Химия. Онлайн учебник → Химические свойства NO2
Оксиды азотной кислоты
Степени окисления в N - от +1 до +5:
N2(+1)O, N(+2)O, N2(+3)O3, N(+4)O2, N2(+5)O5
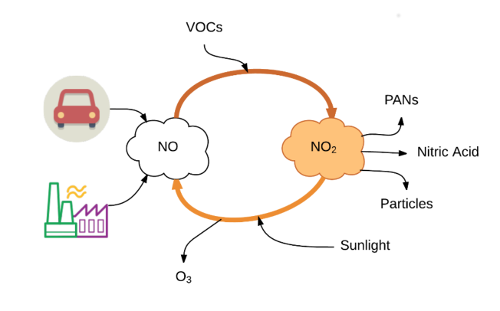
Оксид азота (II) (NO) - бесцветный газ, плохо растворяется в воде. Непосредственно соединяется с кислородом воздуха, создавая при этом бурый газ - оксид азота (IV):
2NO + O2 ⇔ 2NO2
NO2 - газ бурого цвета со специфическим запахом, тяжелее воздуха, ядовитый. Легко превращается в жидкость красноватого цвета, tкип.(NO2) = 21,3 °C. Во время охлаждения жидкого NO2 создаются бесцветные кристаллы, имеющие tпл.(NO2) = -11 °C.
Получение в лаборатории
1. Во время взаимодействия концентрированной HNO3 с медью:
Cu(0) + 4HN(+5)O3 = Cu(+2)(NO3)2 + 2N(+4)O2 + 2H2O
Cu - 2e → Cu(+2) | 1
N(+5) + 1e → N(+4) | 2
2. Во время прожаривания кристаллического нитрата свинца:
2Pb(NO3)2 = 2PbO + 4NO2 + O2
Химические свойства NO2
1. Взаимодействие с водой:
2N(+4)O2 + H2O = HN(+5)O3 + HN(+3)O2
(N (+4) - 1e → N(+5)) + (N (+4) + 1e → N(+3)) = 2N(+4) = N(+5) + N(+3)
3NO2 + H2O (теплая) = 2HNO3 + NO
HNO2 - азотистая кислота
2. Взаимодействие с основаниями (щелочами):
2NO2 + 2NaOH = NaNO3 + NaNO2 + H2O
3. Более свойственная окислительная функция. Он легко окисляет H2SO3 до H2SO4, а йодид-ионы - к свободному йоду:
H2S(+4)O3 + NO2(+4) = H2S(+6)O4 + NO(+2)
2KI- + 2N(+4)O2 = 2KN(+3)O2 + I2
Определение ионов веществ
| Ион или вещество | Реактив | Результат реакции |
| NH4+ | NaOH |
Запах аммиака NH4Cl + NaOH = NaCl + NH3 + H2O |
| PO43- | AgNO3 |
Создается P желтый Na3PO4 + 2AgNO3 = Ag3PO4 + 3NaNO3 |
| NH3 | универсальный индикатор бумага | NH4Cl (t) = NH3 + HCl |
Соли HNO3 - нитраты
Соли HNO3 во время нагрева распадаются, причем продукты распада зависят от положения металла соли в ряде активности металлов:
| Левее от Mg | Mg-Cu | Правее от Cu |
| MNO2 + O2 | MO + NO2 + O2 | M + NO2 + O2 |
Азот: (часть 1) (часть 2) (часть 3)
Автор: Гончаренко Л. И. (ula-books.com.ua)
< Урок 34 | Химия. Онлайн учебник | Урок 36 >
Смотрите также:
Электролиз KCl и K2SO4
Электролиз раствора CuCl2
Электролиз расплава MgCl2