Урок 33. Азот (N2) и соли аммония (NH4)
Химия. Онлайн учебник → Азот и соли аммония
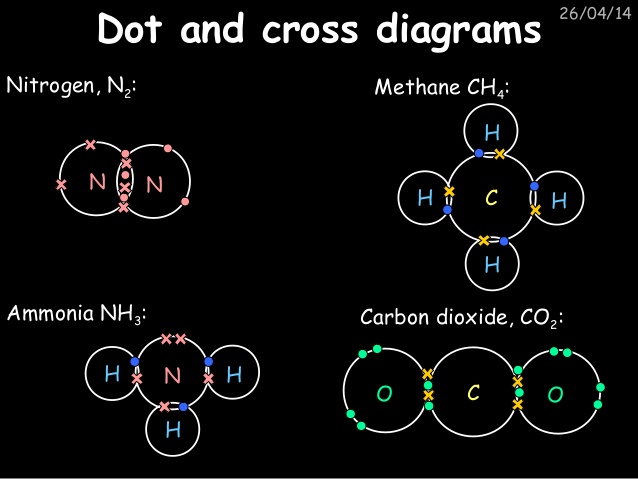
N2 - азот, газ без цвета, запаха, вкуса, легче чем воздух. Низкая растворимость в воде.
Химические свойства
1. Создаются нитриды во время нагревания с металлами:
6Li(0) + N2(0) = 2Li3(+1)N(-3)
2. Взаимодействие с неметаллами:
а) с кислородом при t > 2000 °C или при t = 400 °C при наличии катализатора:
N2(0) + O2(0) (t, к) = 2N(+2)O(-2)
NO - оксид азота (II)
б) с водородом:
N2(0) + 3H2(0) (t, p) (Fe) = 2N(-3)H3(+1)
NH3 - аммиак.
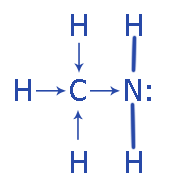
Аммиак (NH3)
NH3 - бесцветный газ с резким запахом, почти вдвое легче воздуха. Чрезвычайно высокая растворимость в воде. Раствор аммиака в воде (25%) называют нашатырным спиртом.
Получение NH3
1. В лаборатории:
2NH4Cl + Ca(OH)2 (t) = CaCl2 + 2NH3 + 2H2O
2. В промышленности:
N2 + 3N2 (t, p) = 2NH3 + Q
Химические свойства
1. Растворение в воде:
NH3 + H2O ⇔ NH4+ + OH- - щелочная среда.
2. Взаимодействие с кислотами:
NH3 + HCl = NH4Cl - хлорид аммония - средняя соль.
NH3 + H3PO4 = NH4H2PO4 - дигидроортофосфат аммония (кислая соль)
2NH3 + H3PO4 = (NH4)2HPO4 - гидроортофосфат аммония (кислая соль).
3NH3 + H3PO4 = (NH4)3PO4 - ортофосфат аммония (средняя соль).
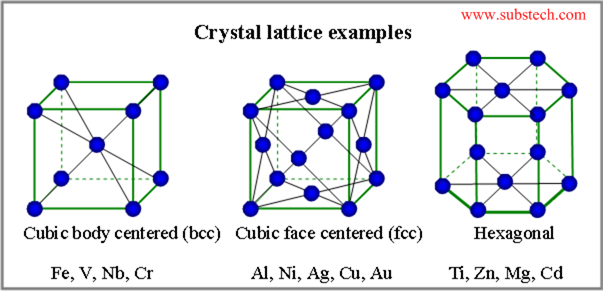
Соли аммония
Кристаллические вещества, которые хорошо растворяются в воде, бесцветные. Их добывают при взаимодействии аммиака или его водного раствора с соответствующими кислотами.
Химические свойства
1. Соли аммония реагируют с другими солями:
NH4Cl + AgNO3 = AgCl + NH4NO3
Ag+ + Cl- = AgCl
2. Взаимодействуют с основаниями:
NH4Cl + KOH = NH3 + KCl + H2O
NH4+ + OH- = NH3 + H2O
3. Во время нагревания соли аммония разлагаются:
а) обратно, если анион соли не является окислителем или проявляет слабые окислительные свойства, например:
NH4Cl ⇔ NH3 + HCl
(NH4)2CO3 ⇔ 2NH3 + CO2 + H2O
б) соли аммония, анионы которых являются окислителями, разлагаются безвозвратно - происходит окислительно-восстановительная реакция:
N(-3)H4N(+5)O3 = N2(+1)O + 2H2O
Азот: (часть 1) (часть 2) (часть 3)
Автор: Гончаренко Л. И. (ula-books.com.ua)
< Урок 32 | Химия. Онлайн учебник | Урок 34 >
Смотрите также:
Бинарные и многоэлементные соединения
Онлайн тесты по химии (с ответами)
Чистые вещества и смеси