Урок 10. Свойства и связь кристаллических решеток
Химия. Онлайн учебник → Свойства и связь кристаллических решеток
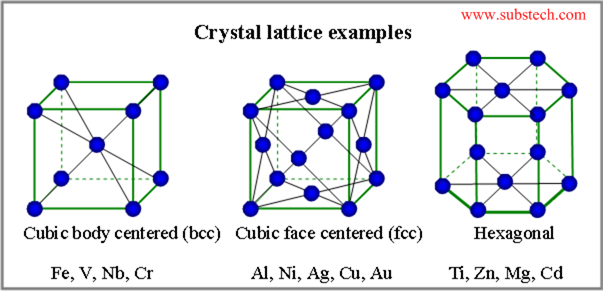
Изображение: www.substech.com.
Кристаллической решеткой вещества называют совокупность ее структурных единиц, что отображает порядок размещения частиц в массе вещества.
Типы кристаллических решеток
Металлическая - отдельные атомы и позитивно заряженные ионы металла, между которыми находится электронный газ. Хим. связь: металлическая.
Свойства: твердые, кроме Hg. Легко- и тугоплавкие, проводят электрический ток, тепло, пластичны.
Молекулярная - молекулы. Хим. связь: соединены между собой силами межмолекулярного взаимодействия; ковалентная полярная и неполярная.
Свойства: незначительная твердость, низкая t плавления, нерастворимы или малорастворимы в воде, их растворы почти не проводят электрический ток (твердый CO2, F2, H2, O2, N2, O3; органические вещества, кислоты, оксиды неметаллов, водородные соединения неметаллов).
Атомная - атомы. Хим. связь: ковалентная неполярная, ковалентная полярная (SiO2, SiC).
Свойства: высокая твердость вещества и температура плавления (алмаз, графит, Si, B), твердые вещества, практически нерастворимы в жидкостях.
Ионная - катионы, анионы. Хим. связь: ионная.
Свойства: уступают веществам с атомной решеткой, но имеют преимущество над веществами с молекулярной решеткой. Имеют сравнительно высокие tпл, обычно не летучие (NaCl, NH4NO3, MgO), не проводят электрический ток в твердом состоянии, а в жидком (расплавленном) состоянии являются электропроводящими.
Электроотрицательность - способность атомов в соединении притягивать к себе электроны. В периодах наблюдается общая тенденция увеличения электроотрицательности элементов, а в группах - ее падения.
Степень окисления - условный заряд, который приобрел атом, если бы все электроны его хим. связей в этом соединении сместились к более электроотрицательному атому.
- Степень окисления может иметь плюсовое или минусовое, целое значение, не превышающее 8.
- Степень окисления элементов в простых веществах равняется 0.
- Алгебраическая сумма степеней окисления всех атомов в веществе равна 0.
- Фтор в соединениях всегда показывает степень окисления -1.
- Степень окисления Водорода в соединениях, как правило, равна +1. Исключение: +1Na-1H. Степень окисления Кислорода в соединениях, обычно, равна -2. Исключение: +1H2-1O2, +2O-1F2.
Автор: Гончаренко Л. И. (ula-books.com.ua)
Химическая связь: (часть 1) (часть 2)
< Урок 9 | Химия. Онлайн учебник | Урок 11 >
Смотрите также:
Кремний (Si). Применение силикатов
Применение простых веществ Углерода
Алкины. Применение ацетилена