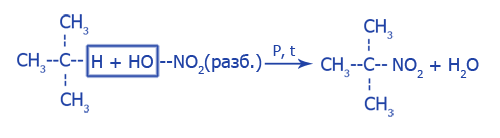Урок 32. Сера. Химические свойства и применение
Химия. Онлайн учебник → Сера. Химические свойства и применение
В простом веществе атомы Серы соединены в цепи, связь между которыми - ковалентная неполярная. Цепи могут быть замкнутыми или открытыми, соответственно - наличие нескольких аллотропных модификаций серы: ромбической, моноклинной и пластической серы.
При нормальных условиях сера - это хрупкое кристаллическое вещество желтого цвета, легкоплавкое, плохо проводит тепло и электрический ток, не растворяется воде. Степени окисления Серы в соединениях: -2, +4, +6.
Химические свойства серы
1. Взаимодействие с металлами (кроме Au, Pt, Ir):
Hg(0) + S(0) = Hg(+2)S(-2)
HgS - сульфид меркурия.
2. Реагирует с неметаллами:
S(0) + H2(0) (t) = H2(+1)S(-2)
H2S - сероводород.
3S(0) + 2P(0) (t) = P2(+3)S3(-2) (без доступа воздуха)
P2S3 - сульфид фосфора (III).
S(0) + 3F2(0) (t) = S(+6)F6(-1)
SF6 - фторид серы (IV).
3. Реагирует с некоторыми сложными веществами:
S + 2H2SO4 (конц.) = 3SO2 + 2H2O
S + 2HNO3 (разб.) = 2NO + H2SO4
S + 6HNO3 (конц.) = 6NO2 + H2SO4 + 2H2O
Применение серы
- В сельском хозяйстве для борьбы с болезнями растений, пчел, домашних животных.
- Для получения сульфатной кислоты.
- В производстве спичек, черного пороха.
- Для вулканизации каучуков.
- В медицине (мази против кожных заболеваний).
Оксиды серы
SO2 - оксид серы (IV), или серный газ, при обычных условиях является бесцветным газом с резким удушающим запахом. Во время охлаждения до -10 °C превращается в бесцветную жидкость.
SO2 создается
1. Во время сжигания серы:
S + O2 (t) = SO2
2. При нагревании меди с концентрированной сульфатной кислотой:
Cu + 2H2SO4 (t) = CuSO4 + SO3 + 2H2O
Химические свойства SO2
1. Во время нагревания взаимодействует с O2:
2SO2 + O2 (t) (к) ⇔ 2SO3
SO3 - сернистый газ.
2. Взаимодействует с H2O:
SO2 + H2O ⇔ H2SO3
H2SO3 - сульфидная кислота, или сернистая кислота.
3. Взаимодействует с основными и амфотерными оксидами:
CaO + SO2 = CaSO3
CaSO3 - сульфит кальция.
4. Взаимодействует с основаниями:
SO2 + 2KOH = K2SO3 + H2O
K2SO3 - сульфит калия.
SO3 - оксид серы (VI), легкое бесцветное вещество (tкип. = 43 °C) с удушливым запахом.
Химические свойства SO3
1. Взаимодействует с H2O:
SO3 + H2O = H2SO4
2. Взаимодействие с основными и амфотерными оксидами:
3SO3 + Al2O3 = Al2(SO4)3
SO3 + CaO = CaSO4
3. Взаимодействие с основаниями:
2NaOH + SO3 = Na2SO4 + H2O
Сульфатная кислота
H2SO4 - сульфатная, или серная кислота, во время обычных условий бесцветная масляная жидкость, без запаха, почти в два раза тяжелее воды, tпл. = +10,3 °C, tкип. = -280 °C. H2SO4 - сильная двухосновная кислота.
Химические свойства
1. Создает соответственные соли с металлами, которые стоят в ряде активности слева от водорода (кроме Pb):
Mg + H2SO4 = MgSO4 + H2
2. Взаимодействие с основными и амфотерными оксидами:
CaO + H2SO4 = MgSO4 + H2
Al2O3 + 3H2SO4 = Al2(SO4)3 + 3H2O
3. Взаимодействие с основаниями:
2NaOH + H2SO4 = Na2SO4 + 2H2O
2Al(OH)3 + 3H2SO4 = Al2(SO4)3 + 6H2O
4. Взаимодействие с солями:
Na2CO3 + H2SO4 = Na2SO4 + H2O + CO2
Соли сульфатной кислоты - сульфаты
1. Во время избытка щелочи создается средняя соль:
2NaOH + H2SO4 = Na2SO4 + 2H2O
2. Во время избытка кислоты создается кислая соль:
NaOH + H2SO4 = NaHSO4 + H2O
Большинство сульфатов растворяется в воде. Во время испарения их растворов часто выделяются кристаллогидраты, например CuSO4 x 5H2O, FeSO4 x 7H2O, Al2(SO4)3 x 18H2O. Качественная реакция на сульфат-ионы:
BaCl2 + Na2SO4 = BaSO4 + 2NaCl
Ba2+ + SO42- = BaSO4
Применение H2SO4 и ее солей
- Производство минеральных удобрений, волокон.
- Получение солей и кислот.
- Получение взрывных веществ.
- Осушение газов.
- Очищение нефтепродуктов.
- Производство лекарственных препаратов.
- Получение органических соединений.
- В свинцовых аккумуляторах.
- Получение красителей.
- В металлургии.
Na2SO4 - в производстве соды и стекла.
K2SO4 - калийное удобрение.
CaSO4 x 2H2O - гипс в медицине, строительстве, в монументальном искусстве.
CuSO4 x 5H2O - сульфат меди (II), пентагидрат, или медный купорос, в сельском хозяйстве.
Автор: Гончаренко Л. И. (ula-books.com.ua)
< Урок 31 | Химия. Онлайн учебник | Урок 33 >
Смотрите также:
Строение энергетических уровней атома
Основные типы химической связи
Периодический закон и периоды